pH крови: какова норма и как измерить его?
Водородный показатель, определяющий кислотность крови, или pH, или маркер кислотно-щелочного равновесия – это постоянная величина.
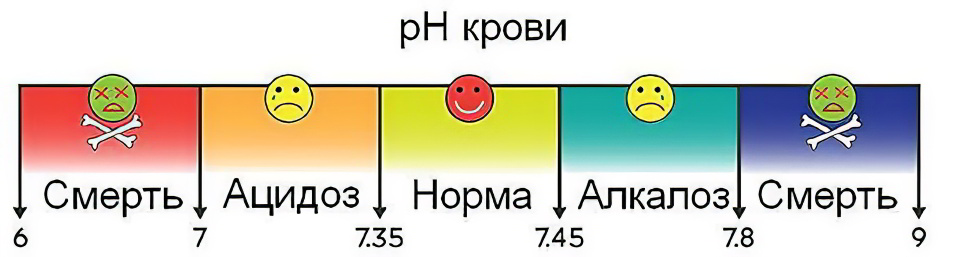
Ее значения в норме находятся в диапазоне от 7,36 до 7,44, обычно – 7,4 единицы.
Смещение показателей в щелочную сторону (алкалоз), или в сторону кислотности (ацидоз) – симптомы неблагополучия, требующие срочного лечения.
Если водородный показатель снижается ниже 7 единиц, или повышается свыше 7,8 единиц, человек находится в пограничном состоянии между жизнью и смертью, где 6,8 с одной стороны, и 8,0 единиц с противоположного отрезка диапазона означают гибель организма.
Кислотно-щелочного равновесия: что это?
Казалось бы, поступление в пищеварительный тракт, и далее в кровь, продуктов с кислой или щелочной реакцией должно менять состав крови. На самом деле, буферные системы организма обеспечивают стабильность кислотно-щелочного равновесия , не допуская колебания за пределы безопасного диапазона.
Перечень буферных систем:
Бикарбонатная (гидрокарбонатная) система – обеспечивает не менее 50% адаптивных способностей системы гемостаза;
Гемоглобиновая система – 35% безопасности;
Система белков крови – 10% буферной емкости;
Фосфатная система – 5-6% буферной безопасности.
Эти системы, поддерживая жизнедеятельность организма, предупреждают сдвиг кислотно-щелочного равновесия в любую сторону, несмотря на то, что организм потребляет продукты разнообразного состава. Буферные системы имеют неистощимый запас прочности, так как их постоянно поддерживает выделительная система, активизирующаяся на уровне рефлексов при необходимости выведения продуктов метаболизма.
Как функционируют системы
Основная гидрокарбонатная система
Гидрокарбонатная система включает в себя два компонента: H2CO3 и NaHCO3. Между ними и поступающими в кровь кислотами и щелочами постоянно происходят химические реакции.
Реакция с сильной щёлочью:
NaOH + H2CO3 → NaHCO3 + H2O
Бикарбонат натрия, образующийся в результате такого взаимодействия, в скором времени выводится мочевыделительной системой.
Нейтрализация поступившей кислоты происходит так:
HCl + NaHCO3 → NaCl + H2CO3
В результате реакции образуется углекислый газ, выводимый лёгкими в окружающую среду.
Бикарбонатная буферная система наиболее чувствительна к изменениям pH, поэтому реагирует на них немедленно.
Гемоглобиновая, белковая и фосфатная системы крови
Гемоглобин крови при помощи красного пигмента реагирует на изменения кислотности, связывая кислород, или отдавая его в окружающие ткани. Кислотность красного пигмента гемоглобина меняется на 0,15 единицы, выступая в зависимости от обстоятельств, как нейтральная соль или как слабая кислота.
Реакция гемоглобина при поступлении в кровь щелочного основания:
NaOH + HHb → NaHb + H2O
Взаимодействие гемоглобина при поступлении в кровь кислоты:
HCl + NaHb → NaCl + HHb
Белковая буферная система участвует в поддержании равновесия pH в зависимости от концентрации и структуры белковых соединений.
Фосфатная система буферной безопасности поддерживает кислотно-щелочной баланс в моче, в межклеточной жидкости, в цитоплазме клетки.
pH разных систем крови человека
Кислотно-щелочной показатель артериальной крови, насыщенной кислородом, на 0,01-0,02 единицы выше такого же показателя венозной крови, в избытке содержащей углекислый газ.
Кислотность плазмы крови, имеющей баланс ионов водорода и гидроксильных ионов, соответствует кислотности крови в целом.
Водородный показатель других сред (сыворотки) может иметь небольшой диапазон значений. Плазма крови, изъятая из системы гемостаза, лишена фибриногена. Её кислотность имеет значение в практическом плане, когда плазма используется для определения группы крови с помощью гемаглюттинирующих сывороток.
Ацидоз и алкалоз крови
Сдвиг водородного баланса в кислую или щелочную сторону может быть компенсированным и некомпенсированным. Он определяется по щелочному резерву – объёму углекислого газа, вытесняемого сильной кислотой из 100 мл плазмы. Норма этого показателя – 50-70 мл CO2.
CO2 ниже 45 мл – некомпенсированный ацидоз;
CO2 выше 70 мл – алкалоз.
Виды алкалоза:
Газовый – возникает при высотной болезни, при гипервентиляции лёгких, провоцируется повышенной отдачей лёгкими углекислого газа, переходит в гипокапнию;
Негазовый – различают алиментарный алкалоз, поступающий с пищей, и метаболический алкалоз, связанный с изменениями метаболизма.
Виды ацидоза:
Газовый – провоцируется замедленной отдачей CO2 легкими, переходит в гиперкапнию;
Негазовый (алиментарный) – возникает при накоплении продуктов метаболизма, при поступлении их из ЖКТ;
Первичный ренальный – возникает при нарушении реосорбции в почечных канальцах, сопровождающихся потерей щелочей.
При значительном отклонении водородного показателя от нормы требуется квалифицированная медицинская помощь. При его пребывании в предельных значениях диапазона, при удовлетворительном самочувствии важно самому пациенту обращать внимание на состояние своего здоровья.
Основные причины нарушения pH – употребление «вредных» продуктов, алкоголя, курение. Если пациент не владеет информацией, он не обратит внимания на своё здоровье, пока не окажется в состоянии острой патологии.
Нормализовать кислотно-щелочной баланс можно при помощи диетического питания, но при возвращении прежнего образа жизни показатели pH вернутся к прежним значениям.
Для поддержания показателя в пределах нормы требуется соблюдение правил здорового питания, режима, выполнение оздоровительных мероприятий.